内容概况:近年来,政策因素持续深刻影响着我国仿制药行业的发展格局。药品上市许可持有人制度、药品专利纠纷早期解决机制等政策的落实与完善,进一步优化了行业生态,推动了竞争格局的重塑。2024年,我国过评/视同过评的仿制药产品数量达2998个,较2023年增加1008个,同比增长50.65%,呈现逐年增长的趋势自药品上市许可持有人制度试点并全面实施以来,委托生产逐渐成为企业加快仿制药市场布局的关键策略之一。2024年,在过评/视同过评的仿制药产品中,委托生产的占比达到33%,较2020年的12%实现显著提升,亦呈现出逐年递增的趋势,反映出行业分工协作与资源配置的进一步深化。
相关上市企业:泰格医药(300347)、华海药业(600521)、海王生物(000078)、山河药辅(300452)、京新药业(002020)、信立泰(002294)、恒瑞医药(600276)、华润双鹤(600062)、海正药业(600267)、ST人福(600079)等。
相关企业:合肥智汇医药科技有限公司等。
关键词:仿制药一致性评价的意义、仿制药一致性评价行业相关政策、仿制药一致性评价行业产业链、化学仿制药市场规模及在整体药品和化学药规模中占比、仿制药参比制剂纳入品种数、过评/视同过评的药品批文数、过评/视同过评仿制药品种数量、过评/视同过评的仿制药产品及委托生产占比、仿制药一致性评价行业发展趋势
一、仿制药一致性评价行业概述
仿制药一致性评价是指对已经批准上市的仿制药,按与原研药品质量和疗效一致的原则,分期分批进行质量一致性评价,就是仿制药需在质量与药效上达到与原研药一致的水平。
仿制药一致性评价的流程从确定参比制剂开始,经过药学研究、体外溶出度试验、生物等效性研究,到数据整理与报告撰写,最终完成申报与审批,并进行持续监测与再评价。整个流程强调了仿制药与参比制剂在质量、疗效和安全性上的高度一致性,确保仿制药能够达到与原研药品相同的临床效果。通过以上流程,仿制药的一致性评价旨在确保仿制药与原研药品在疗效和安全性上具有高度一致性,从而保障患者用药的安全性和有效性。

仿制药一致性评价的意义包括:(1)有利于提高药品的有效性;(2)有利于降低百姓用药支出,节约医疗费用;(3)有利于提升医药行业发展质量,进一步推动医药产业国际化;(4)有利于推进供给侧结构性改革。

二、仿制药一致性评价行业政策
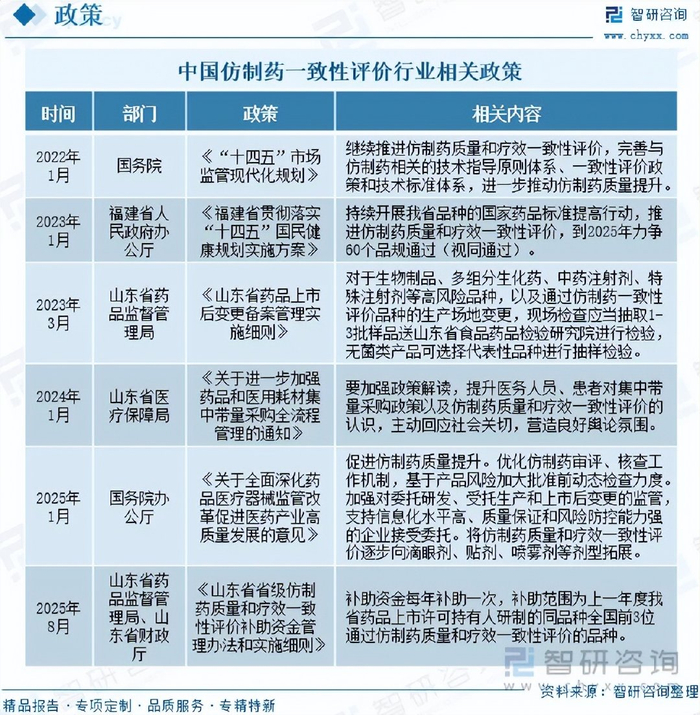
随着医药科技不断进步,药品审评标准在不断提高,过去的药品审评标准没有强制要求仿制药与原研药质量和疗效一致,所以有些药品在疗效上与原研药存在一定差距,需要改进提高。近年来,国家和地方政府相继出台政策推动仿制药一致性评价,不仅能提升药品质量,促进仿制药与原研药的相互替代,而且还有助于降低药品价格,减轻群众用药负担,保障药品可及性。例如,2025年1月,国务院办公厅印发《关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》,促进仿制药质量提升。优化仿制药审评、核查工作机制,基于产品风险加大批准前动态检查力度。加强对委托研发、受托生产和上市后变更的监管,支持信息化水平高、质量保证和风险防控能力强的企业接受委托。将仿制药质量和疗效一致性评价逐步向滴眼剂、贴剂、喷雾剂等剂型拓展。2025年8月,山东省药品监督管理局、山东省财政厅印发《山东省省级仿制药质量和疗效一致性评价补助资金管理办法和实施细则》,提出补助资金每年补助一次,补助范围为上一年度我省药品上市许可持有人研制的同品种全国前3位通过仿制药质量和疗效一致性评价的品种。
三、仿制药一致性评价行业产业链
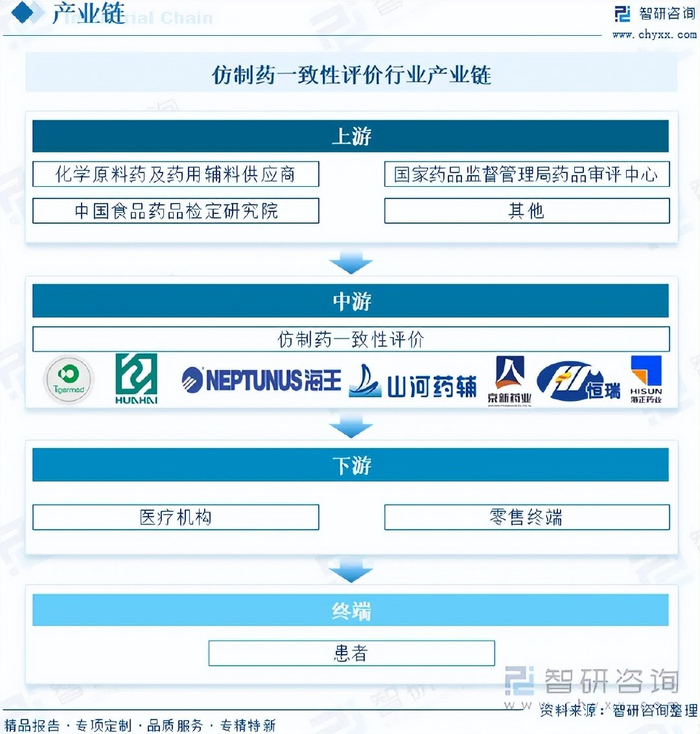
仿制药一致性评价产业链上游为化学原料药及药用辅料供应商、国家药品监督管理局药品审评中心(CDE)、中国食品药品检定研究院(NIFDC)等。产业链中游为通过评价的仿制药生产企业。产业链下游为已通过一致性的仿制药上市流通,进入医疗机构和零售终端,最终服务于患者用药需求。
相关报告:智研咨询发布的《中国仿制药一致性评价行业市场现状调查及发展趋向研判报告》
四、仿制药一致性评价行业发展现状
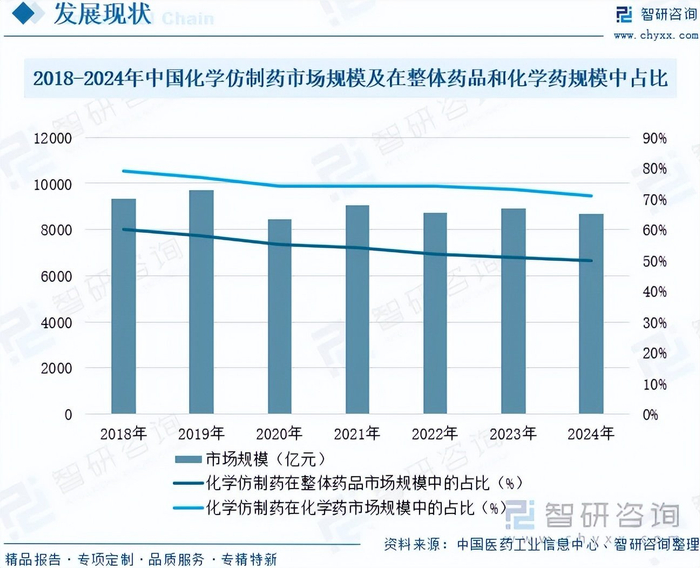
仿制药,即通用名药物(也称非专利药、学名药)是指原研药物(也称专利药、品牌药)专利到期或得到专利授权后,其他制药企业参照相关标准开发生产的,具有相同活性成分、剂型、给药途径和治疗作用,在临床治疗上被认为与原研药物可以等效替代的药物。仿制药是我国医药工业的重要组成部分,对于降低药品费用、减轻患者负担、增强药品可及性具有十分重要的意义。长期以来,仿制药的发展为我国医药产业的转型升级提供有力支撑。促进仿制药研发,提高药品供应保障能力,是加快我国由制药大国向制药强国跨越的坚实基础。我国是仿制药大国。在供给侧,仿制药品种数超4000个(按药品名称计),从事化学仿制药的生产企业超过4000家。在需求侧,2024年中国化学仿制药市场规模为8683亿元,同比下降3%。自2018年以来,化学仿制药市场进入持续调整周期,增长中枢持续下移。
随着我国高质量发展扎实推进,医药产业进入结构转型升级时期。近年来,化学药市场机构不断优化调整,化学仿制药市场份额持续走低。2024年中国化学仿制药在整体药品市场规模中的占比从2018年的60%下降至50%;在化学药市场规模中的占比从2018年的79%下降至71%。
化学仿制药的高质量发展是健全完善我国药品供应保障体系的重要工作内容。开展仿制药一致性评价,可以使仿制药在质量和疗效上与原研药一致,在临床上可替代原研药,这不仅可以节约医疗费用,同时也可提升我国的仿制药质量和制药行业的整体发展水平,保证公众用药安全有效。化学仿制药一致性评价于2016年正式启动。2017年,国务院办公厅发布《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,提出力争用5至10年左右时间基本完成对已上市药品进行一致性评价工作。同年年底,首批通过一致性评价的药品名单公布。2019-2020年,国家药品监督管理局发布《关于开展化学药品注射剂仿制药质量和疗效一致性评价工作的公告》,启动对已上市的化药注射剂仿制药进行一致性评价。2023年,《仿制药质量和疗效一致性评价受理审查指南(征求意见稿)》发布,进一步完善了化学仿制药一致性的审批指导。2025年,《关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》发布,将仿制药质量和疗效一致性评价逐步向滴眼剂、贴剂、喷雾剂等剂型拓展。
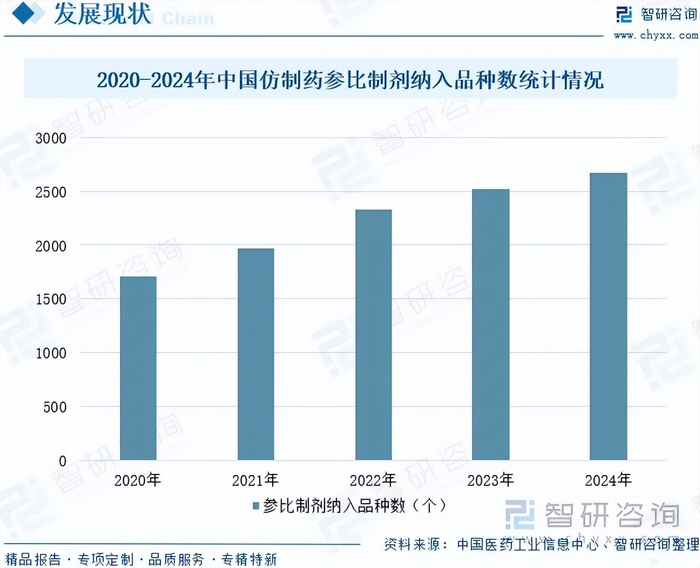
仿制药参比制剂目录是开展仿制药一致性评价的重要依据。《关于开展仿制药质量和疗效一致性评价的意见》中明确提出建立我国仿制药参比制剂目录集,助力一致性评价工作开展。《仿制药参比制剂目录(第一批)》于2017年发布,截至2024年底,国家药监局已累计发布八十七批,累计涉及2672个品种(按目录序号计)。2024年,仿制药参比制剂目录递选工作引入动态调整机制,年内公布了第一批调出参比制剂目录品种清单。首批调出清单仅涉及盐酸氨溴索吸入溶液1个品种(序号:27-251)。该品种因不符合中国药典吸入制剂通则关于“吸入液体制剂应为无菌制剂”的要求而被调出参比目录。
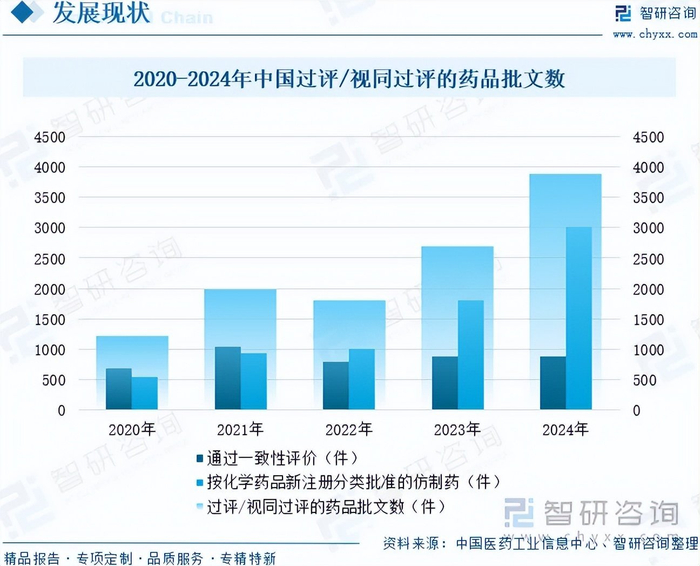
截至2024年底,通过一致性评价以及按化学药品新注册分类批准的仿制药品(视同通过)批文累计已超过10000件,过评/视同通过品种数累计超1100个。2024年中国过评/视同通过的批文合计3891件,较2023年大幅增加。按化学药品新注册分类批准的仿制药批文数量超3000件,成为过评批文的主要构成。另一方面,2024年针对已上市药品的一致性评价工作同样持续推进,年内共计超过300余个品种的过评批文878件。自2017年首批过评药品名单公布以来,先后对已上市的口服制剂与注射制剂开展一致性评价工作,累计已有700余个品种的4500余件批文产品通过评价。2024年存量批文产品的过评数量较2021年有所回落,其中年内首次通过一致性评价的品种数从前期的200余种下降至71种。与此同时,年内一致性评价补充申请数量出现下降,从2023年的1006件减少至659件。从过评数据和过评申请上看,口服与注射制剂存量产品的过评工作已过高峰期,滴眼剂、贴剂、吸入剂等其他剂型的一致性评价或将成为重点。
注:本文节选出自智研咨询发布的《2026年中国仿制药一致性评价行业政策、产业链、发展现状、重点企业及趋势研判:仿制药一致性评价工作逐步推进,过评/视同过评的产品数量达2998个[图]》行业分析文章,如需获取行业文章全部内容,可进入智研咨询官网搜索查看。
更多关于仿制药一致性评价产业的深度研究及全面数据,请关注智研咨询官网或公众号(智研咨询),您也可以咨询了解智研咨询重磅发布的《中国仿制药一致性评价行业市场现状调查及发展趋向研判报告》。

本《报告》从2025年全国仿制药一致性评价行业发展环境、整体运行态势、运行现状、进出口、竞争格局等角度进行入手,系统、客观的对我国仿制药一致性评价行业发展运行进行了深度剖析,展望2025年中国仿制药一致性评价行业发展趋势。《报告》是系统分析2025年度中国仿制药一致性评价行业发展状况的著作,对于全面了解中国仿制药一致性评价行业的发展状况、开展与仿制药一致性评价行业发展相关的学术研究和实践,具有重要的借鉴价值,可供从事仿制药一致性评价行业相关的政府部门、科研机构、产业企业等相关人员阅读参考。
智研咨询专注产业咨询十五年,是中国产业咨询领域专业服务机构。公司以“用信息驱动产业发展,为企业投资决策赋能”为品牌理念。为企业提供专业的产业咨询服务,主要服务包含精品行研报告、专项定制、月度专题、可研报告、商业计划书、产业规划等。提供周报/月报/季报/年报等定期报告和定制数据,内容涵盖政策监测、企业动态、行业数据、产品价格变化、投融资概览、市场机遇及风险分析等。
>>>查看更多:股市要闻