(来源:远东资信)
本文所称化学制药是指以基础化学原料、经化学修饰的天然化合物或微生物发酵获得的具有明确化学结构且符合药用标准的代谢产物为起始物料,在GMP条件下通过化学合成、生物催化等手段定向构建目标分子,经分离纯化制得化学原料药或进一步制成制剂的全过程,涵盖从原料药到制剂的一体化质量监管,但排除运用重组DNA等技术的生物制药。行业监管框架以国家药监局为核心,统筹CMC全生命周期监管,协同医保局、卫健委等部门,形成"法律-行政法规-部门规章-政策文件与技术指导原则"四级架构,2026年新修订《药品管理法实施条例》进一步强化全链条监管与创新支持。
从化学制药行业外部环境看,2025年末60岁及以上人口占比达23.0%,人口老龄化加速推动慢病与肿瘤需求刚性增长,高血压、糖尿病患者合计近5亿人。当前政策呈现"医保支付控费与药品创新并重"双轨特征,前十一批集采覆盖490种药品、平均降价超50%,仿制药利润空间持续压缩;同时商保创新药目录探索建立,为创新药开辟补充支付通道。技术创新方面,AI制药有望缩短研发周期30%-50%,ADC药物、小核酸药物等新技术路线加速发展。国际化进程上,2025年原料药出口额428.7亿美元,创新药License-out交易总额创1357亿美元新高。
行业运行总体平稳,2024-2025年全国规模以上医药制造企业营收增速分别为0.37%、-1.69%,利润总额同比增速由负转正,但企业亏损面由2018年14.44%升至28.74%。细分领域中,申万行业下化学原料药企业仍在调整,2025年前三季度营收同比下降6.92%、利润下降10.73%;申万行业下化学制剂企业表现稍好,营业同比下降0.36%,利润同比增长1.37%。出口方面,2025年,原料药出口额同比微降0.3%,制剂出口额同比增长27.29%。创新药支持政策体系历史性升级,2025年批准创新药76款创历史新高,化学药品占比61.8%,新版医保与商保双目录落地执行。展望"十五五"时期,行业将呈现"总量趋稳、结构优化、创新驱动、绿色转型"特征。
行业债券发行人方面,目前16家企业共有存续债券22只、余额236.25亿元,以AAA级企业发行为主。数据显示,企业规模分化显著,复星医药、新和成等6家总资产超百亿元,而共同药业、灵康药业等6家营收不足10亿元。盈利能力与杠杆方面,共同药业、灵康药业、东亚药业、博瑞医药2025年前三季度投入资本回报率低于1.5%,共同药业、华北制药总债务资本化比率超50%。偿债能力上,共同药业、华海药业等2025Q3现金短债比低于0.5倍,共同药业、灵康药业、东亚药业等经营现金流偿债能力偏弱。
综合来看,规模偏大的化学制药企业偿债能力相对较好,而少量规模偏小企业面临盈利与偿债双重压力,特别是高杠杆的共同药业、经营造血能力不佳的灵康药业与东亚药业。展望未来一年,预计多数发行人信用状况将保持相对稳定,但规模偏小企业的结构性风险仍值得关注。
正文
一、化学制药行业概况
(一)行业定义
本文中的化学制药,是指以基础化学原料、经化学修饰的天然来源化合物,或微生物发酵获得的具有明确化学结构且符合药用标准的代谢产物为起始物料,在符合药品生产质量管理规范(Good Manufacturing Practice,GMP)要求的条件下,采用经注册批准的生产工艺,通过化学合成、生物催化等手段定向构建目标分子,并经分离纯化制得化学原料药;或进一步通过制剂工艺制成化学药制剂(包括放射性药品等特殊管理药品)的全过程。该过程须符合药品注册管理要求,并通过验证的分析方法确保产品结构确证、杂质可控、质量稳定,最终满足其作为药品用于人体的安全、有效、质量可控的预期用途。本定义不包括通过重组DNA技术、细胞培养技术或基因编辑技术制备的生物制品,但上述生物制品中经化学合成或修饰的小分子组分(通常指分子量小于5000道尔顿的化合物,如抗体偶联药物(Antibody-Drug Conjugates,ADC)中的毒素载荷(Payload)等)适用本定义。此外,参考国际监管实践,鉴于化学合成多肽、寡核苷酸等大分子化学药物通常按化学药品管理,本文将其归类至化学制药。
上述关于化学制药定义的表述体现了如下特点:
一是,从起始物料与物质维度(Input)看,上述定义明确了化学制药的“三大基石”,涵盖了从纯人工合成到天然产物改造的全光谱。
(1)基础化学原料: 纯合成路径,从简单的小分子构建复杂结构。
(2)经修饰的天然化合物: 半合成路径,利用自然界已有的复杂骨架(如青蒿素)进行化学修饰以增强药效或降低毒性。
(3)微生物代谢产物: 生化结合路径,虽然由微生物产生,但强调“明确化学结构”,这将其与成分复杂的粗制生物提取物区分开来。
二是,从技术与工艺维度 (Process)看,上述定义强调了分子构建的“定向性”与“纯化过程”。
(1)定向构建:通过化学合成(Organic Synthesis)或生物催化(Biocatalysis,如酶催化)实现目标分子的定向构建,并经验证的分析方法确保结构确证与杂质可控。
(2)制药工程全链条:涵盖从原料药 (Active Pharmaceutical Ingredient,API) 的合成到制剂 (Drug Product) 加工的全过程,符合“原料药-制剂”一体化质量监管要求。
三是,从监管与质量标准 (Quality & Regulatory)维度看,上述化学制药的定义将研发阶段的结构确证与生产阶段的GMP控制整合为统一体系。
(1)体系要求:必须符合GMP要求,确保生产过程的可追溯性与一致性。
(2)合规要求:必须遵循注册批准的工艺,任何变更均需申报批准。
(3)核心三要素:结构确证(明确化合物化学结构)、杂质可控(杂质在安全限度内)、质量稳定(产品在储存条件下保持质量属性)。这三点共同保障药品的核心价值,即安全、有效、质量可控。
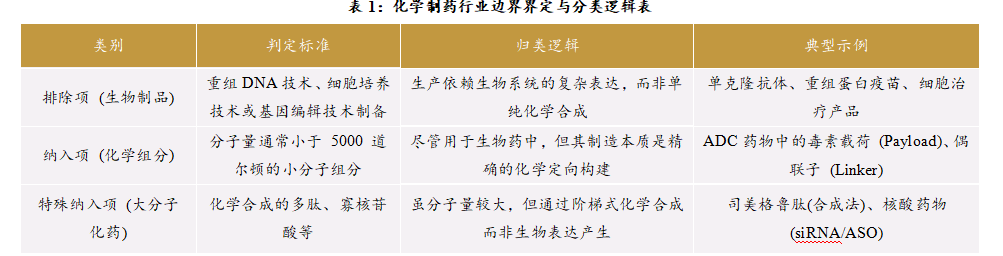
四是,从边界界定与分类逻辑 (Boundary)看,上述定义较好地处理了化学药与生物药之间日益模糊的边界。
相关边界界定与分类逻辑的再梳理,见下表1。
(二)行业监管框架与核心监管法规及政策文件
1.行业监管框架
国家药品监督管理局(简称国家药监局或NMPA)是我国药品监管的主管部门,负责拟订药品监管政策规划,组织起草法律法规草案与部门规章。NMPA统筹化学药品的CMC(化学、生产和控制)全生命周期监管,通过其直属专业技术机构(药品审评中心、食品药品审核查验中心、药品评价中心等)对CMC资料进行技术审评,实施药品注册审批(含化学原料药与制剂关联审评审批)、上市后变更管理、上市后安全性监测与再评价、国家药品标准制修订,并对生产环节是否持续符合GMP要求及经核准的生产工艺开展监督检查(含境内及境外生产现场检查)。
作为协同监管部门,国家医疗保障局负责药品价格、招标采购及支付标准管理,牵头组织药品集中带量采购、开展国家医保谈判、动态调整《国家医保药品目录》,旨在保障药品的经济性与可及性。国家卫生健康委员会侧重于临床端管理,牵头会同相关部门制定《国家基本药物目录》,指导医疗机构合理用药,监测药品短缺信息,牵头负责短缺药品临床需求监测,会同相关部门做好供应保障,并推动公立医院用药结构改革。
此外,国家市场监督管理总局负责药品领域的反垄断、反不正当竞争执法;工业和信息化部负责医药工业产业规划、短缺药品生产供应保障及国家医药储备管理;财政部负责药品监管部门预算及中央财政专项资金管理、医保补助资金及药品集中采购财政专户管理。
2.行业核心监管法规与政策文件
我国化学制药监管体系目前大致可以从"法律-行政法规-部门规章-政策文件与技术指导原则"四级架构来看,以下做简要分析。
一,在基础法律层面,适用《中华人民共和国药品管理法》(2019年修订,简称《药品管理法》)。
《药品管理法》是我国药品监管的根本大法,2019年修订确立了以“四个最严”(最严谨的标准、最严格的监管、最严厉的处罚、最严肃的问责)为核心的监管理念,对化学制药的关键要求包括:
在药品分类上,根据《药品管理法》第2条,药品包括中药、化学药和生物制品等,其分类以法律列举方式呈现。
在药品上市许可持有人(MAH)制度上,根据《药品管理法》第30条,药品上市许可持有人(MAH)为取得药品注册证书的企业或药品研制机构等,需对药品研制、生产、经营、使用全过程的安全性、有效性、质量可控性负责。该制度打破了“生产许可与上市许可绑定”的传统模式,允许研发机构直接持有药品注册证书,激发了创新活力。
在药品研制上,要求化学制药的研制需符合药物非临床研究质量管理规范(GLP)和药物临床试验质量管理规范(GCP)。根据《药品管理法》第19条,药物临床试验应当经国务院药品监督管理部门批准;生物等效性试验实行备案管理。在药品注册时,需提供“真实、充分、可靠的数据、资料和样品”(《药品管理法》第24条),证明其安全性、有效性和质量可控性。
在药品生产上,根据《药品管理法》第43-44条,从事药品生产活动,应当遵守药品生产质量管理规范(GMP);药品应当按照国家药品标准和经药品监督管理部门核准的生产工艺进行生产。生产药品所需的原料、辅料需符合药用要求,直接接触药品的包装材料和容器需符合保障人体健康、安全的标准(《药品管理法》第45-46条)。
特别地,在《药品管理法》中,对化学原料药提出了特殊规定:国务院药品监督管理部门在审批药品时,对化学原料药一并审评审批,对相关辅料、直接接触药品的包装材料和容器一并审评,对药品的质量标准、生产工艺、标签和说明书一并核准。
二,在行政法规层面,即将适用《中华人民共和国药品管理法实施条例》(2026年修订版)。
2026年1月16日,国务院公布修订后的《中华人民共和国药品管理法实施条例》,自2026年5月15日起施行。修订遵循"人民至上、生命至上"原则,落实药品安全监管"四个最严"要求,强化全链条监管;支持药品创新,促进药品产业高质量发展;坚持问题导向,有针对性地细化补充制度措施。修订重点包括完善药品研制和注册制度(支持以临床价值为导向的药品研制创新,对符合条件的儿童用药品、罕见病治疗用药品给予市场独占期),加强药品生产管理(强化药品上市许可持有人(MAH)主体责任,严格药品委托生产管理,规定境内上市药品境外生产需符合我国要求),规范药品经营和使用(完善药品网络销售管理制度,细化医疗机构制剂管理制度),严格药品安全监管(明确监督检查措施,细化假药认定情形,规定质量抽查检验流程)。
三,在部门规章层面,适用《药品注册管理办法》(2020年修订版)、《药品生产监督管理办法》(2020年修订版)和《药品生产质量管理规范》(2010年修订版及后续配套补充规定,GMP)。
《药品注册管理办法》规范了化学药品的注册审批流程,明确了药品上市许可的申请路径,包括创新药申请、仿制药申请(可基于生物等效性试验豁免部分临床试验)等,同时细化了注册资料要求,推动药品注册的规范化与高效化。《药品生产监督管理办法》明确了药品生产活动的准入要求,规定从事药品生产活动需取得药品生产许可证,同时要求药品上市许可持有人建立药品质量保证体系,严格遵守GMP要求,确保生产过程持续符合法定要求。《药品生产质量管理规范》(GMP)是化学制药生产环节的核心技术规范,涵盖了生产环境、设备管理、物料控制、生产流程、质量检验等生产环节的要求,通过验证、记录追溯等手段保障药品生产的一致性与质量稳定性。
四,在政策与技术指导原则层面,适用集采、仿制药质量提升、监管改革等政策文件以及注册指导、研究与质量控制等方面的技术指导原则文件。
《国务院办公厅关于推动药品集中带量采购工作常态化制度化开展的意见》(国办发〔2021〕2号)是指导药品集中带量采购从试点探索转向常态化、制度化开展的指导性政策文件,明确以"招采合一、量价挂钩"为核心机制,推动国家组织与地方协同推进的集中采购工作,旨在降低药价、保障供应、净化行业生态并促进医药行业高质量发展。《国务院办公厅关于全面深化药品医疗器械监管改革 促进医药产业高质量发展的意见》(国办发〔2024〕53号)对临床急需的重点创新药和医疗器械实行“提前介入、一企一策、全程指导、研审联动”机制,深化药品审评审批制度改革,包括在部分地区开展试点优化创新药临床试验审评审批流程,将审评审批时限由60个工作日缩短为30个工作日,将仿制药质量和疗效一致性评价逐步向滴眼剂、贴剂、喷雾剂等剂型拓展,构建覆盖全生命周期的监管服务体系,推动医药产业向高端化、智能化、国际化发展。之后发布的《化学药品仿制药上市许可申请模块二药学资料撰写要求 (试行)》(2025年),旨在提高仿制药申报资料质量,促进仿制药质量提升。
《化学药品注册分类及申报资料要求》(2020年)是国家药监局2020年6月发布的配套文件,将化学药品注册分为5类:1类(境内外均未上市的创新药)、2类(境内外均未上市的改良型新药)、3类(境内申请人仿制境外上市但境内未上市原研药品)、4类(境内申请人仿制境内上市原研药品)、5类(境外上市的药品申请在境内上市),并明确了各类药品的申报资料要求,核心特点是强调临床价值导向、区分创新药与改良型新药标准、优化仿制药审评要求(如3类仿制药需境外原研药作参比,4类仿制药需以境内原研药为参比),推动化学药品注册分类与国际接轨。
化学制药相关技术指导原则体系以国际协调的ICH(国际人用药品注册技术协调会)指南和国家药监局(NMPA)及药品审评中心(CDE)制定的技术指南为主要支柱。截至2024年底,中国已采纳实施ICH现行有效指导原则(涵盖质量、安全性、有效性和多学科四大类别)70余个,实施水平与欧美日等ICH监管机构成员相统一;同时CDE累计发布数百个技术指导原则(2024年新增数十个),形成覆盖化学药、生物制品、中药全品类,贯穿非临床、临床、CMC、上市后研究全生命周期的指导原则体系,为化学药品研发、审评和监管提供科学规范的技术支撑。
二、近年化学制药行业外部环境分析
1.需求支撑刚性用药长期增长:人口老龄化与疾病谱升级
截至2025年末,60岁及以上人口占全国人口的23.0%(其中65岁及以上人口占比15.9%),人口老龄化加速推动慢病与肿瘤等大病种需求刚性扩张,其中高血压、糖尿病患者合计近5亿人,年新发肿瘤病例超480万;叠加居民健康意识与支付结构升级,化学药在抗感染、心血管、代谢、神经系统等领域具备长期需求底座;同时院外渠道、自费市场崛起,为高价值品种提供更稳定的盈利场景。
2.医保支付政策重构:集采常态化与商业保险破局
医保支付是化学制药行业的核心变量,直接决定企业盈利空间。当前政策呈现"控费与创新并重"的双轨特征:一方面,前十一批药品集采,覆盖490种药品,平均降价超过50%,仿制药利润空间持续压缩,加速淘汰低效企业。另一方面,创新激励政策(如“优质优价”原则)推动企业加大研发投入,创新药上市速度显著提升,行业集中度持续提高,头部企业主导创新药布局。2025年医保目录调整首次建立商保创新药目录,引入商业保险支付高值创新药,有望在医保‘保基本’之外形成补充性支付机制,为创新药提供新的商业化路径。
3.技术创新重塑产业逻辑:AI技术突破与新技术路线形成
技术创新重塑化学制药产业逻辑,AI技术突破与ADC、小核酸药物等新技术路线启动大力发展,推动产业向精准创新转型。AI制药赋能研发全流程,有望将传统研发周期缩短30%-50%、降低研发成本20%以上,实现精准高效研发。同时,新技术路线进入爆发期,ADC药物靶向性持续升级,国内企业在特色靶点实现全球领跑,成为肿瘤治疗核心赛道;小核酸药物借助GalNAc递送技术突破,适应症从罕见病拓展至减重等大慢病领域,商业化进程加速。多维技术协同重构产业全链条,推动行业向高端化升级。
4.国际化进程加速:原料药出口与创新药License-out(对外授权)并行
在原料药领域,中国作为全球最大出口国(2025年出口额428.7亿美元,占全球30%以上份额),通过技术升级与产能扩张持续强化竞争力。大宗原料药(如抗生素、维生素)凭借规模化生产与成本优势,占据印度、东南亚等新兴市场核心份额;特色原料药(如多肽激素、GLP-1中间体)则依托技术突破打开高端市场,2025年多肽类原料药出口额同比激增81.7%,成为新增长极。面对欧盟《关键药物法案》等贸易壁垒,中国企业通过本地化生产(如华海药业在越南建厂)与质量升级(通过PIC/S认证)应对挑战,维持供应链韧性。
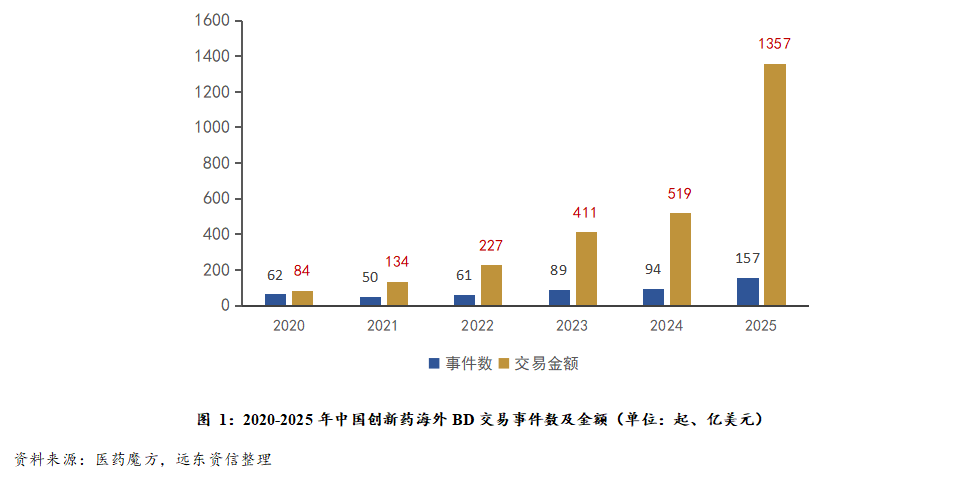
在创新药License-out领域,中国药企通过技术授权实现全球价值链跃迁。2025年创新药对外授权交易总额高达1357亿美元(见下图1),创历史新高,恒瑞医药、百济神州等头部企业通过“自主出海+联合开发”模式,将ADC等前沿技术资产注入国际市场。交易结构从单一首付款向“里程碑+分成”深化,形成“研发-商业化-收益共享”闭环。同时,NewCo模式(如恒瑞GLP-1管线授权海外子公司)通过股权绑定与风险共担,推动中国药企深度参与全球研发与商业化网络。
三、近年化学制药行业整体运行态势与未来发展趋势展望
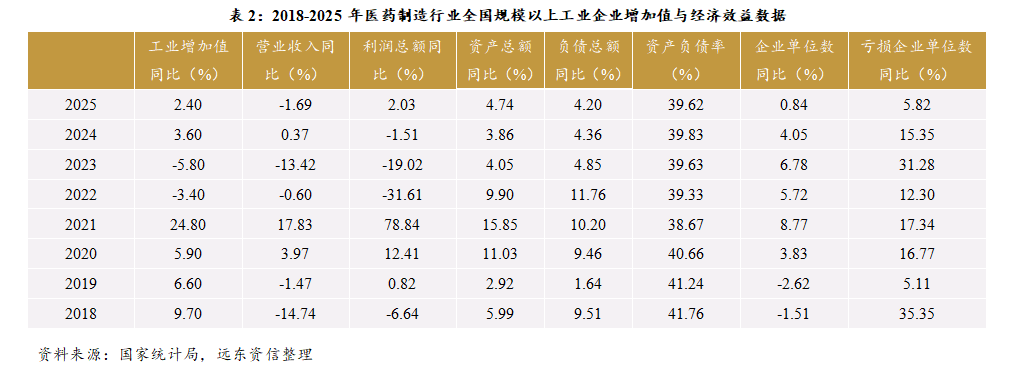
1.2024-2025年医药制造大类行业总体平稳
国家统计局统计数据显示,2024年、2025年规模以上医药制造企业的营业收入同比增速分别为+0.37%、-1.69%,分别较同期其工业增加值同比增速低3.23个百分点、4.09个百分点,价格因素对营收造成不小的负面影响。2024年到2025年,利润总额同比增长由负转正,扭转了2022年至2024年连续三年的下滑趋势。从近几年数据来看,规模以上医药制造企业的资产负债率相对稳定;不过,其中亏损企业数量同比增速持续多年高于规模以上医药制造企业整体同比增速,即企业亏损面不断扩大,具体看,企业亏损面由2018年的14.44%增加至28.74%,几乎是翻倍。
总体看,2022年以来,随着疫情的结束,疫苗与一些医药用品、卫生材料销量明显下降,叠加化学原料药的供给侧调整(产能与产量有所压缩),使得医药制造品的销量出现调整;另外,随着国家与地方药品集中带量采购政策的不断深入实施,纳入集中采购范围的产品覆盖面持续扩大,药品价格明显下降。这两方面因素,给医药制造企业营业收入和利润带来了不小的压力。就趋势来说,2025年,医药制药业多项数据也呈现振荡走稳态势。
2.化学原料药企业仍在调整,化学制剂企业总体表现稍好
预计截至2025年末,我国化学制药的市场规模大约在一万亿元左右。从数据可获性考虑,同时为了讨论方便,这里用A股上市公司口径的申万行业来进行讨论。
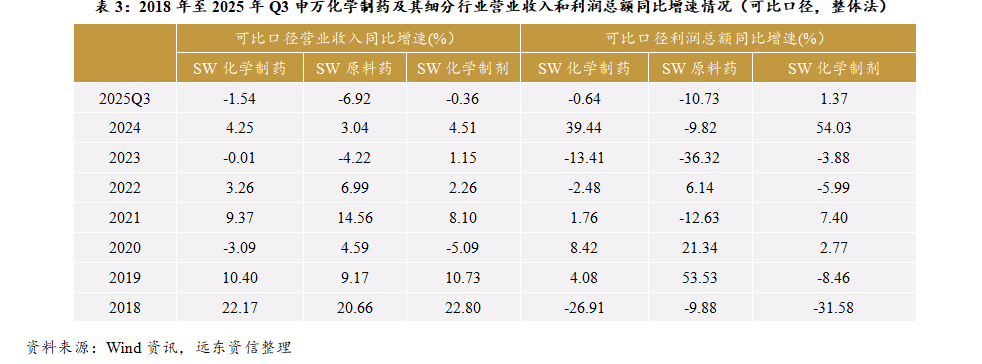
从营业收入看,2024年、2025年前三季度申万化学制药行业的营业收入同比增速(可比口径)分别为+4.25%、-1.54%,分别较2024年、2025年规模以上医药制造企业的营业收入同比增速高3.88个百分点、0.15个百分点。其中,2024年、2025年Q3申万化学原料药行业的营业收入同比增速(可比口径)分别为+3.04%、-6.92%,分别较同期化学制药所有企业的营业收入同比增速低1.21个百分点、5.38个百分点。2024年、2025年Q3申万化学制剂行业的营业收入同比增速(可比口径)分别为+4.51%、-0.36%,分别较同期化学制药所有企业的营业收入同比增速高0.26个百分点、1.18个百分点。从利润总额看,2024年、2025年Q3申万化学原料药行业的利润总额同比(可比口径)都有10%左右的下跌,2023年以来在利润上的承压尚未得到实质性扭转;而申万化学制剂行业的利润总额同比增速(可比口径)在2024年大幅反弹+54.03%之后,在2025年又小幅走高+1.37%,要明显好于整体化学制药的表现。
3.2024年恢复性增长后,原料药与制剂出口2025年有所分化
2024年我国化学制药出口呈现恢复性增长态势,原料药与制剂双轮驱动态势初步形成。中国医药保健品进出口商会数据显示,全年化学原料药出口额达429.8亿美元,同比增长5.1%,成功扭转2023年下滑20%的颓势,回归常态增长轨道;化学制剂出口额达69.5亿美元,同比增长10%,出口量增速高达16.9%,成为拉动行业增长的新引擎。从产品结构看,原料药仍占据化学制药出口的主导地位,但制剂占比持续提升,标志着出口结构向高附加值方向转型。区域市场方面,亚洲以188.1亿美元稳居原料药最大出口市场,北美和拉丁美洲分别以12.4%和14.1%的增速成为增长亮点,而非洲市场以18.9%的增速展现新兴潜力。从出口国别看,印度和美国仍是我国原料药出口前两大市场。我国对印度出口原料药61.3亿美元,对美国出口原料药45.2亿美元,同比增速分别为-1.0%和+12.0%。总体看,全年化学制药出口呈现明显"量增价减"特征,原料药出口均价下降12.0%,制剂均价下降5.8%,反映出国际市场竞争加剧与产能过剩压力。
2025年我国化学原料药与制剂出口增速走势分化显著。原料药出口维持规模稳定但增长乏力,2025年全年出口额428.7亿美元,同比微降0.3%,较2024年5.1%的增速明显回落,行业进入"以价换量"的深度调整期;维生素类价格走势先涨后跌,抗生素类产品面临价格下行压力,肝素类价格较2021年历史高点回落超三分之二,尽管出口量保持增长,但均价下行压力持续制约出口额提升。受益于全球糖尿病、肥胖症等发病率上升及GLP-1类药物需求激增,多肽类激素原料药2025年出口额达9.0亿美元,同比大幅增长81.7%。2025年化学制剂出口展现“量价齐升”态势,全年出口额88.41亿美元,同比增长27.29%,出口量增长17.71%。区域市场方面,受加征关税的影响,2025年对美制剂出口金额11.62亿美元,同比增长1.01%,对美出口制剂金额占制剂出口总额比重降至13.14%,较2024年下跌约3.4个百分点;对欧盟(不含英国)制剂出口仍然占比最高,同比增长70.4%,相较2024年上升约10个百分点。
4.国家大力支持创新药高质量发展
2025年我国创新药支持政策体系实现历史性升级,构建起覆盖研发、审评、准入、支付、国际化的全链条保障机制。政策层面,2024年7月国务院常务会议审议通过的《全链条支持创新药发展实施方案》奠定顶层设计基础,2025年政策落地提速:2025年6月,国家医保局与国家卫健委联合印发《支持创新药高质量发展的若干措施》,明确5个维度16条具体举措,明确通过医保数据赋能研发、鼓励加大创新药投资、实施目录准入政策辅导及国家科技重大专项支持等措施,激发创新药研发活力,其中增设商业健康保险创新药品目录,纳入创新程度较高、有一定临床价值且超出基本医保保障范围的创新药,供商业健康保险和医疗互助等多层次医疗保障体系参考使用;7月,《2025年国家基本医疗保险药品目录及商业健康保险创新药品目录调整工作方案》征求意见,标志着"医保+商保"双目录体系建设启动,为创新药开辟基本医保之外的市场化支付通道。审评审批环节,国家药监局将符合条件的创新药临床试验审批时限从60个工作日压缩至30个工作日,2025 年上半年即批准创新药 43 款,全年批准创新药 76 款,创历史新高。2026年1月1日起,新版《国家基本医疗保险、生育保险和工伤保险药品目录》以及《商业健康保险创新药品目录》已正式落地执行,新版国家医保药品目录新增114种药品,其中50种1类创新药。
近三年我国1类创新药审批呈现爆发式增长态势,化学药创新药表现尤为突出。2023年批准40个1类创新药,2024年增至48个,2025年跃升至76个,三年累计达164个,实现从"跟跑"到"并跑"的跨越。化学药创新药占比稳居半壁江山,2025年批准的76个创新药中,化学药品47个(占比61.8%),其中38个为国产创新药,国产占比达80.85%。首创新药(First-in-class,FIC)实现突破,2025年批准的11个首创新药中4个为国产自主研发,标志着原始创新能力萌芽。
政策效能与市场反馈形成正向循环。医保支付端,2024年新增91个药品中33个实现"当年获批、当年纳入",创新药从上市到纳入医保周期从5年压缩至1年左右,约80%的创新药可在上市2年内获得医保支付。随着《支持创新药高质量发展的若干措施》的印发,商保衔接机制突破,创新药支付通道多元格局将逐步形成。资本市场响应积极,2025年A股与港股合计近20家生物医药企业上市。区域政策配套密集出台,北京、上海、广东等十余个省(市)在临床试验加速、伦理审查互认、入院使用保障等方面形成差异化竞争格局。
5.化学制药未来发展趋势
党的二十届四中全会审议通过的《中共中央关于制定国民经济和社会发展第十五个五年规划的建议》(以下简称《建议》)对加强药品安全工作,支持创新药和医疗器械发展等提出明确要求。
展望2026年及"十五五"时期,我国化学制药行业将呈现"总量趋稳、结构优化、创新驱动、绿色转型"的发展特征。从供给端看,原料药产能调整进入深水区,在"反内卷"政策推动下,低端同质化产能加速出清,高端特色原料药和专利原料药占比提升,行业集中度预计明显提升;化学制剂领域,随着集采常态化推进和一致性评价范围稳步拓展,仿制药利润空间持续压缩,倒逼企业向"原料药+制剂"一体化转型,通过成本控制保障供应链稳定性。从需求端看,人口老龄化加剧和慢病患病率上升推动市场需求刚性增长,但支付端医保"保基本"定位与高价创新药可及性矛盾仍存,商保目录落地进度将成为关键变量。
技术创新与绿色制造将成为行业高质量发展的核心驱动力。在创新药领域,化学药与生物技术融合加速,靶向治疗、免疫调节、长效缓释等新型制剂成为研发重点;在生产方式上,连续流化学、微反应器技术、机械化学等绿色工艺加速普及,人工智能辅助分子设计和工艺优化逐渐成为标配,推动能耗不断降低、污染排放持续减少。国际化方面,随着欧洲产能理性化和美国供应链重构,中国原料药全球份额有望稳中有升;制剂出口从"以价换量"向技术授权转型,License-out模式持续扩容。整体而言,化学制药行业将从规模扩张转向质量效益,在绿色化、智能化、国际化三重变革中构建新竞争优势。
四、化学制药行业债券发行人信用状况分析及展望
1.化学制药行业债券发行人与相关债券概况
目前我国在交易所与银行间债券市场共有16家化学制药行业债券发行人。其中,原料药企业8家,均为民营企业;化学制剂企业4家,除1家为外资企业外,其余3家为民营企业;原料药与制剂一体化企业4家,民企与地方国企各2家。在这16家企业中,除江苏联环药业集团有限公司以外,其余均为上市公司。从发行人委托评级的主体级别来看,复星医药、科伦药业为AAA级,华北制药为AA+级,华海药业、健友股份为AA级,花园生物、奥锐特、博瑞医药、美诺华为AA-级,东亚药业、九典制药、微芯生物为A+级,共同药业为A级,灵康药业为A-级;联环药业和新和成没有公开级别。在这16家企业中,有12家为高新技术企业。
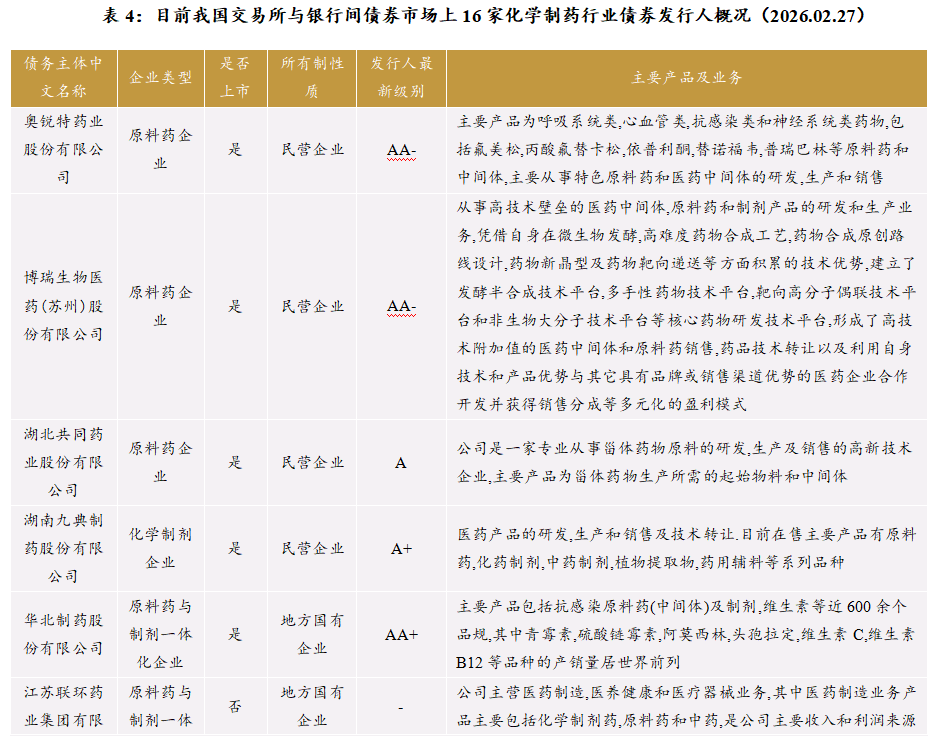
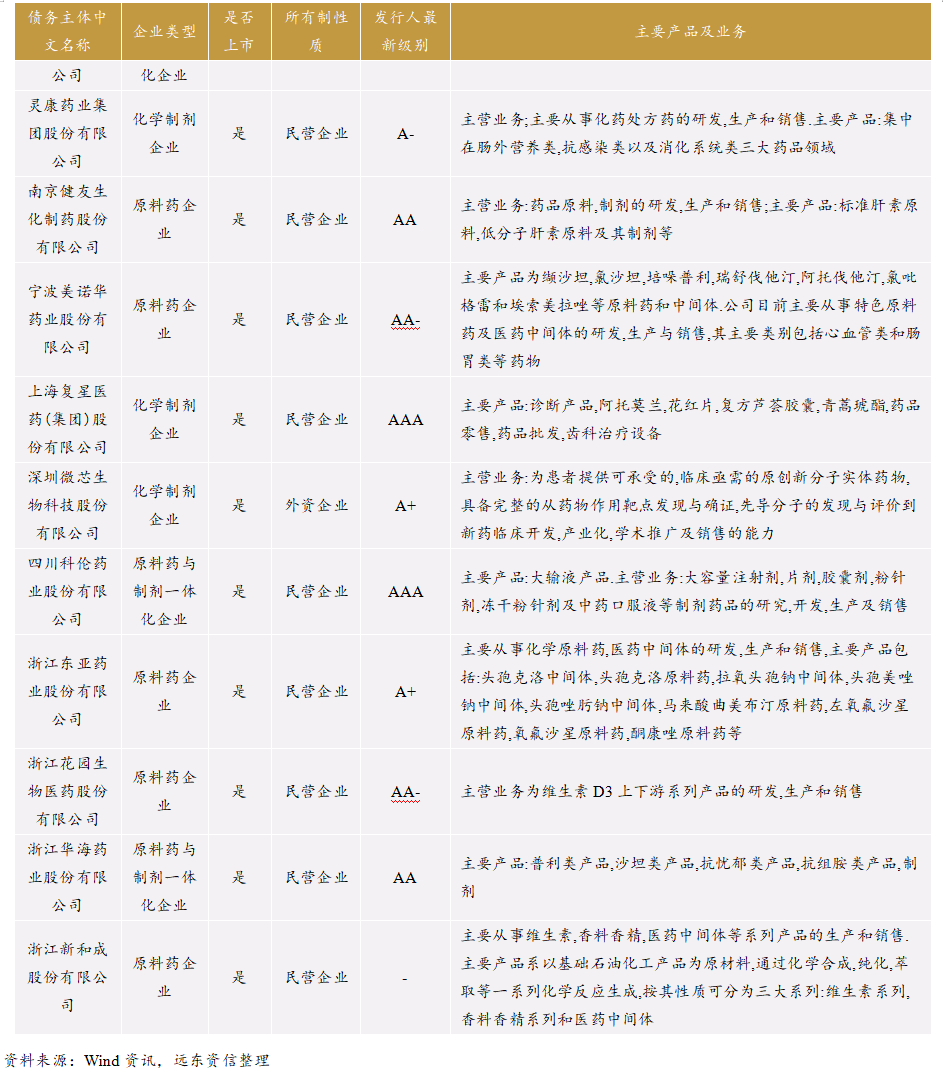
从化学制药行业债券来看,上述16家化学制药企业目前共有存续债券22只,最新债券余额为236.25亿元。这些债券简要情况分析如下:
(1)这些债券中,有7只债券在2026年年内到期,涉及债券的余额共计80.38亿元;有3只债券在2027年到期,涉及债券的余额共计59.56亿元。
(2)AAA级的复星医药、科伦药业旗下的7只债券,目前余额为142.6亿元;博瑞医药旗下的2只债券,在增信后债项级别为AAA级,目前余额为14.86亿元。这9只债券在目前化学制药行业债券余额总额中占比66.65%。
(3)AA级及以下的有评级债券,共计10只,全部为转债,目前余额为63.8亿元。另外,还有华北制药发行的中票1只,目前余额为5.0亿元。
(4)22只债券中有10只为科技创新债券,目前余额为134.04亿元。
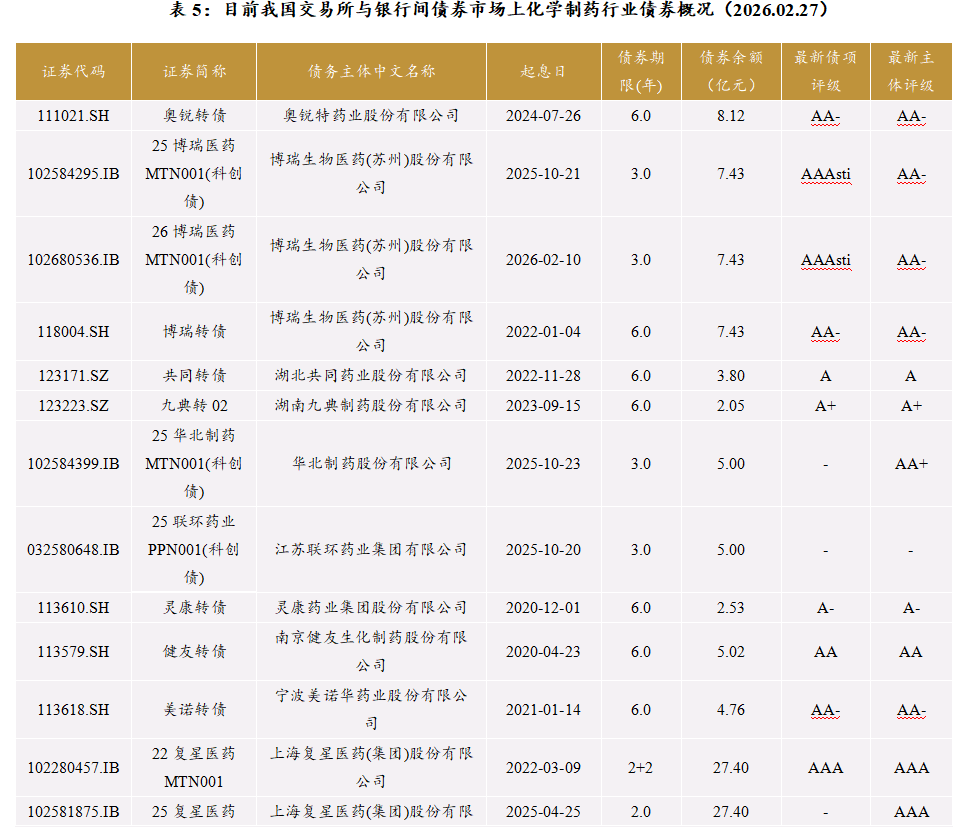
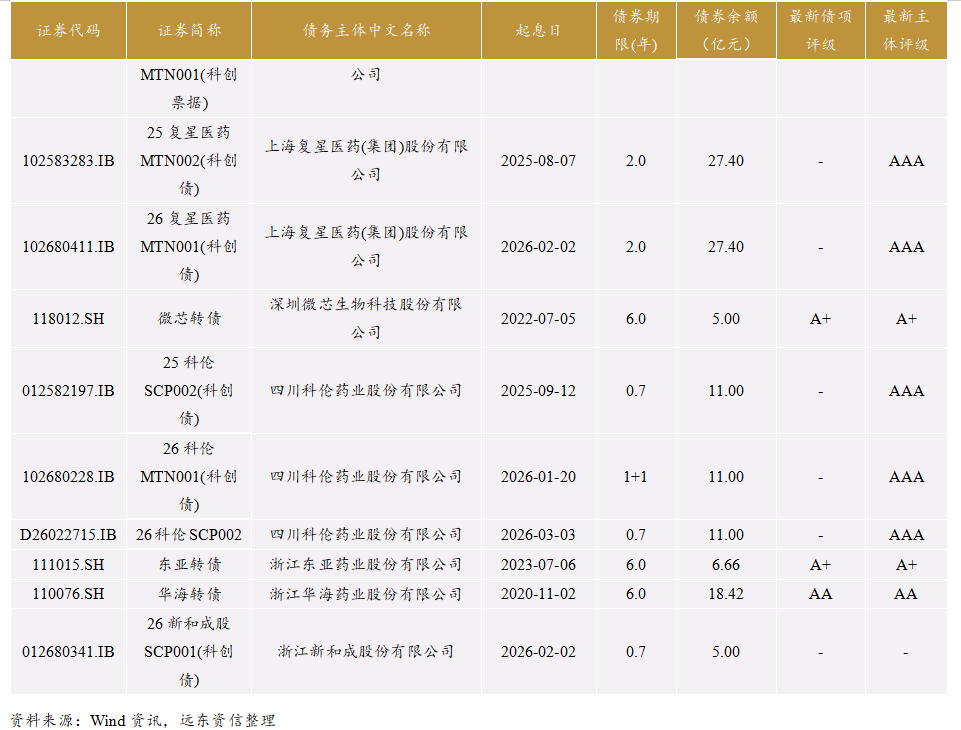
2.化学制药行业债券发行人信用分析
(1)规模
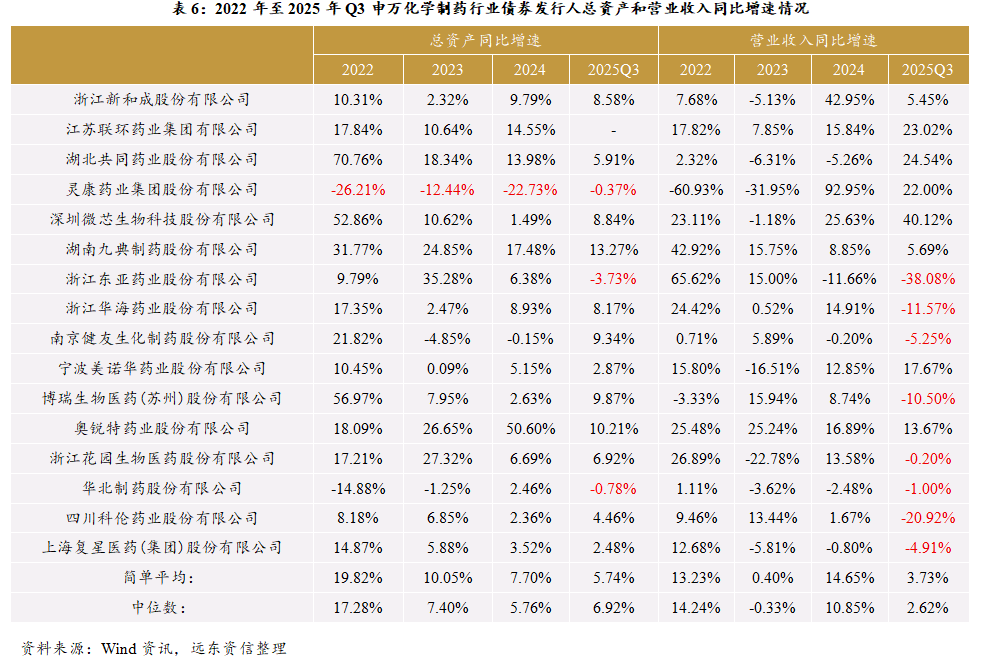
在化学制药行业债券发行人中,2025年第三季度末总资产规模超过100亿元的仅有复星医药(1181.21亿元)、新和成(450.94亿元)、科伦药业(401.04亿元)、华北制药(215.37亿元)、华海药业(211.53亿元)、健友股份(103.07亿元)等6家企业。2025年前三季度营业收入超过60亿元的仅有复星医药(293.93亿元)、新和成(166.42亿元)、科伦药业(132.77亿元)、华北制药(74.85亿元)、华海药业(64.09亿元)等5家企业;而2025年前三季度营业收入低于10亿元的有共同药业(4.55亿元)、灵康药业(2.82亿元)、微芯生物(6.74亿元)、东亚药业(5.96亿元)、博瑞医药(8.74亿元)和花园生物(9.36亿元)。
从总资产同比增速的简单平均值与中位数数据看,化学制药行业债券发行人总体资产规模在2022年末大幅增长后,在2023年末、2024年末和2025年第三季度末保持了中速增长,同比增速约在6%-7%左右波动。有三家企业在2025年第三季度末的总资产规模,出现了同比负增长:(1)灵康药业资产规模在2022-2024年持续明显缩水,其在2025年第三季度末资产规模同比下降幅度收窄,但仍微跌;(2)东亚药业资产规模在连续三年扩张后,在2025年第三季度末出现同比3.73%的回落;(3)华北制药近几年的资产规模在持续调整中,其2025年第三季度末资产规模同比微跌。
从营业收入同比增速的简单平均值与中位数数据看,化学制药行业债券发行人总体营业收入同比在2022年和2024年超过10%,在2023年和2025年前三季度同比增长偏弱。仅从2025年前三季度营业收入增速来看,结构分化比较明显,其中东亚药业、华海药业、博瑞医药、科伦药业等4家企业的营收同比增速下滑超过10%。
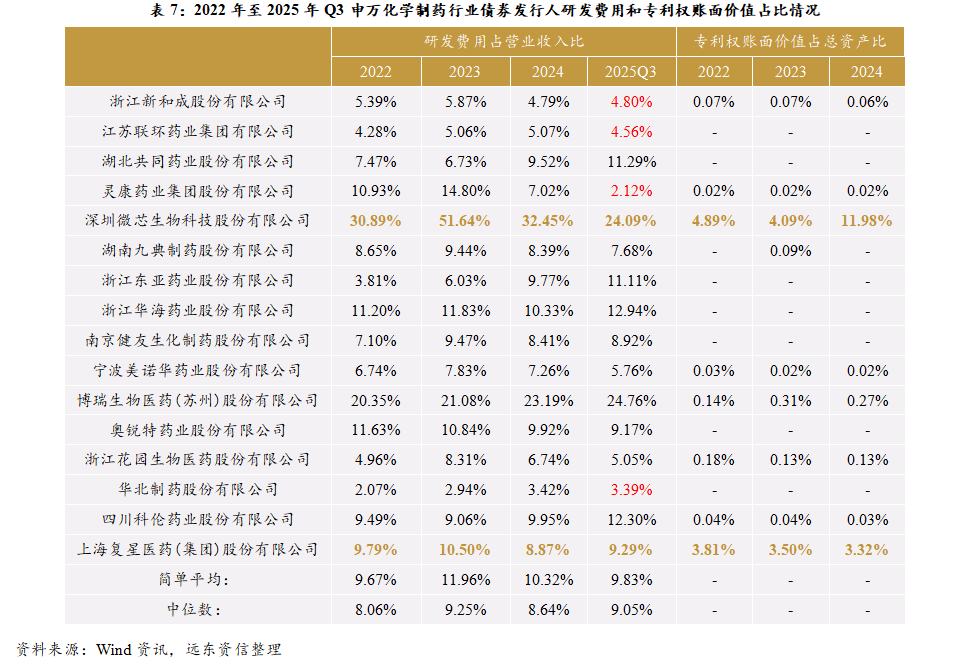
(2)研发费用与专利价值
综合研发费用占营业收入比和专利权账面价值占总资产比看,近年来微芯生物的研发与专利上支出水平相对较高,博瑞医药和复星医药也有不错的表现,而华北制药的研发费用持续不高,专利权账面价值无数据可查。
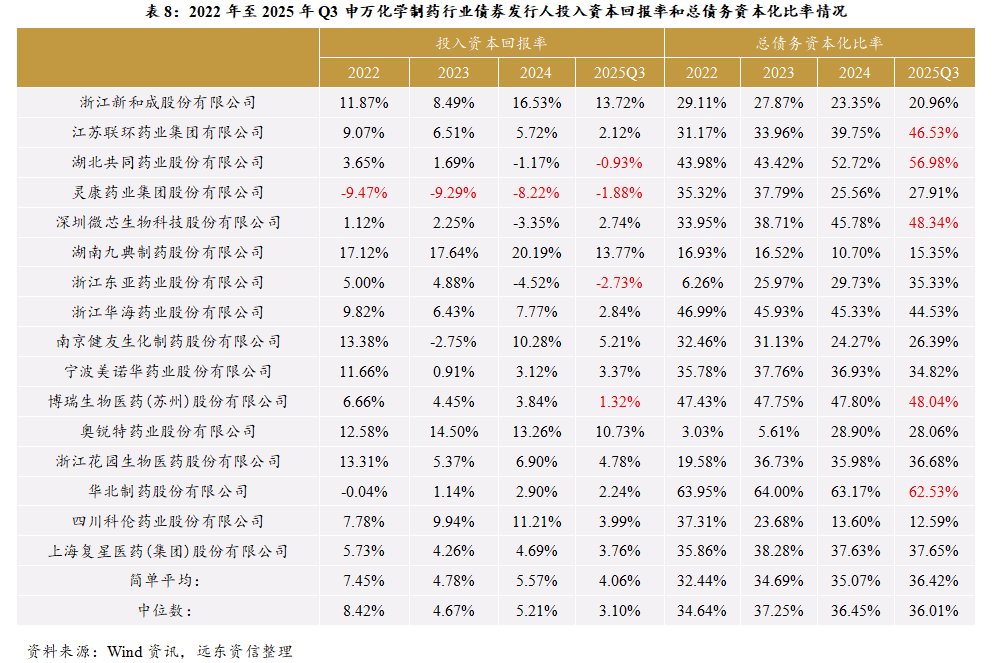
(3)盈利能力与财务杠杆
结合近年无风险资产利率来看,投入资本回报率(年化)如低于2.0%,则这可视为盈利能力较差的表现。当然,如果企业仅某一年的投入资本回报率(年化)低于2.0%,而大部分年份的投入资本回报率显著高于2%,这可能也不会显著拖累其偿债能力。
一般来说,总债务资本化比率会明显低于资产负债率。如果某家企业的总债务资本化比率超过50%,其资产负债率很可能会超过60%。
从2025年前三季度的投资资本回报率看,低于1.5%(年化相对于低于2.0%)的企业有四家,分别是共同药业、灵康药业、东亚药业和博瑞医药。其中,灵康医药2022-2024年这三年的投入资本回报率为很大的负值,较弱的盈利能力值得关注。
从2025年第三季度末的总债务资本化比率看,显著高于50%的企业有两家,分别是共同药业和华北制药;低于50%但接近于50%的企业有三家,分别是联环药业、微芯生物、博瑞医药。
上述公司中,共同药业2024年以来,投入资本回报率持续偏弱,总债务资本化比率持续高于50%,该企业或面临不小的债务偿还压力。
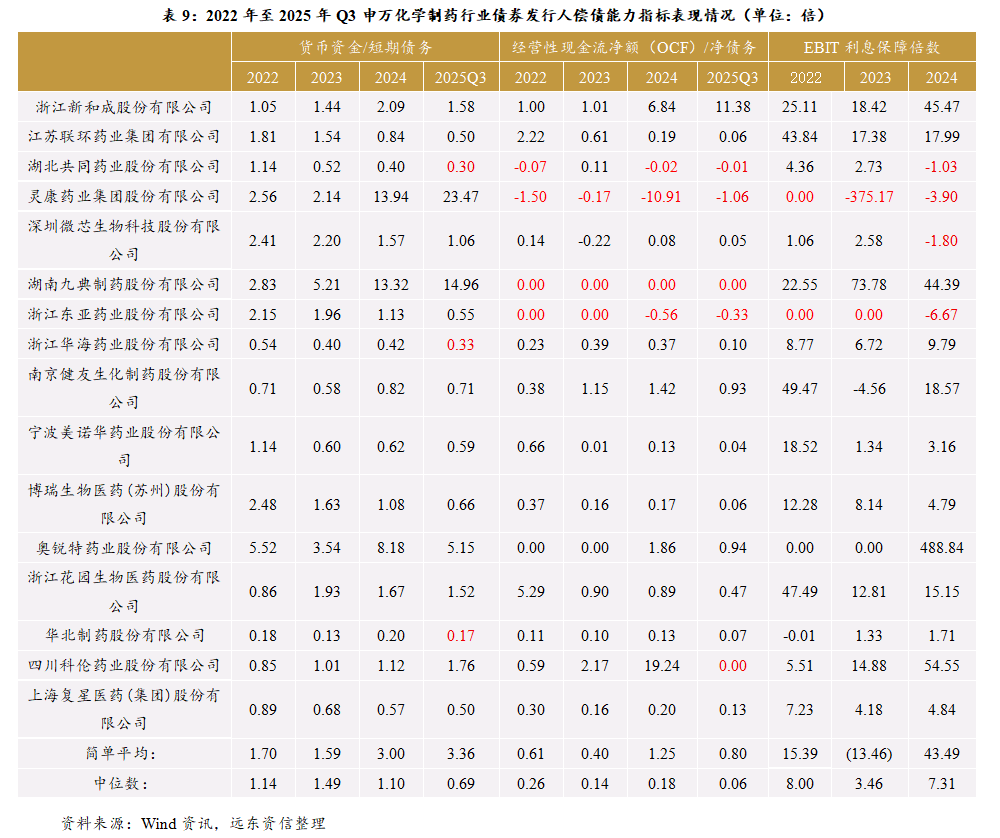
(4)偿债能力
“货币资金/短期债务”指标,在某种程度上来说,衡量的是账面现金对短期债务的即时偿还能力,更偏向从某一角度来考察企业流动性。“经营性现金流净额(OCF)/净债务”指标,考察的是考虑账面现金后(净债务等于付息债务减去货币资金),企业通过自身业务经营造血能力创造的现金流来偿还债务的能力;如果该指标持续多年表现很差,这表明其自身业务经营造血能力很差(某一年表现差,可能还不能充分说明这一点)。“EBIT利息保障倍数”指标考察的是用息税前盈利来偿还债务利息的能力,一般来说,在企业持续经营假定条件下,用“EBIT利息保障倍数”指标来分析会优于“EBITDA利息保障倍数”;此外,该指标得数小于1.0倍或表明通过其当年经营盈利来进行利息偿付面临困难。
从2025年Q3的“货币资金/短期债务”指标来看,共同药业、华海药业、华北制药的读数小于0.5倍,分别为0.3倍、0.33倍和0.17倍,账面现金上的即时流动性或相对弱。从2022-2024年、2025年Q3的“经营性现金流净额(OCF)/净债务”指标来看,共同药业、灵康药业、九典制药和东亚药业表现欠佳,通过其自身经营造血能力来偿还债务能力偏弱。从2022-2024年的“EBIT利息保障倍数”指标来看,灵康药业和东亚药业表现欠佳,通过其当年经营盈利来进行利息偿付面临较大压力(另:正如前文所述,2025年前三季度这两家公司的投入资本回报率均负值)。
3.小结与展望
综合上述分析来看,在债券发行人中,我国规模偏大的化学制药企业偿债能力相对较好,而少量规模偏小的化学制药企业或面临不小的盈利与偿债能力压力,特别是高财务杠杆的共同药业、在通过自身业务经营成果来偿债上能力不佳的灵康药业、东亚药业。
展望未来一年,预计多数化学制药行业债券发行人的信用状况将保持相对稳定,但规模偏小的化学制药企业的结构性风险仍值得关注。
简奖平,远东资信研究院研究与发展部研究员,注册国际投资分析师,清华大学、对外经济贸易大学双硕士。
姚怀国,远东资信研究院研究与发展部研究员,中国社会科学院研究生院国民经济学硕士。
>>>查看更多:股市要闻